應用層是計算機網絡體系結構中的最高層,直接面向用戶和應用程序,負責提供網絡服務接口。常見的應用層協議包括HTTP、FTP、SMTP、DNS等。本文以HTTP協議為例,通過圖解和簡明解析,幫助讀者快速掌握應用層核心概念,輕松應對期末考試。
1. 應用層的基本概念
應用層位于TCP/IP模型或OSI模型的最頂層,其主要功能是為應用程序提供網絡通信服務。例如,當你在瀏覽器中輸入網址訪問網頁時,應用層協議(如HTTP)就會開始工作。
2. 圖解HTTP協議的工作流程
HTTP(超文本傳輸協議)是應用層中最常用的協議之一,用于在Web瀏覽器和服務器之間傳輸數據。以下是HTTP請求-響應過程的簡化圖解:
- 用戶發起請求:用戶在瀏覽器輸入URL(如http://example.com)。
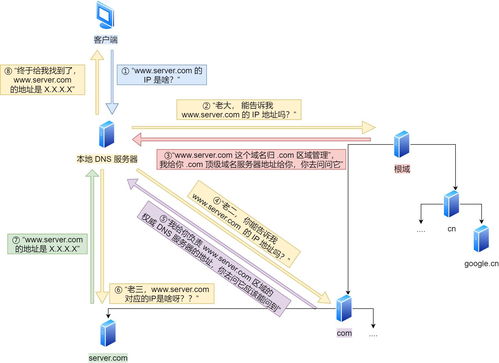
- DNS解析:瀏覽器通過DNS協議將域名解析為IP地址。
- 建立TCP連接:瀏覽器與服務器通過TCP三次握手建立可靠連接。
- 發送HTTP請求:瀏覽器構建HTTP請求報文,包含方法(如GET或POST)、頭部信息和可選正文。
- 服務器處理請求:服務器接收請求,解析并返回HTTP響應報文,包含狀態碼(如200 OK)、頭部和響應正文(如HTML頁面)。
- 瀏覽器渲染:瀏覽器接收響應,解析HTML并顯示網頁內容。
- 關閉連接:完成數據傳輸后,通過TCP四次揮手釋放連接(HTTP/1.1默認使用持久連接以減少開銷)。
3. HTTP關鍵特性解析
- 無狀態協議:HTTP本身不保存用戶狀態,但可通過Cookie或Session實現狀態管理。
- 請求方法:GET(獲取資源)、POST(提交數據)、PUT(更新資源)、DELETE(刪除資源)等。
- 狀態碼:200(成功)、404(未找到)、500(服務器錯誤)等,幫助快速診斷問題。
4. 應用層與計算機系統服務的關系
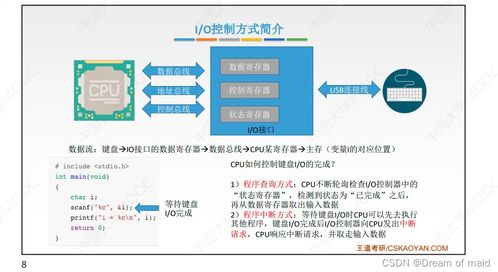
應用層協議依賴于下層協議(如傳輸層的TCP/UDP)和操作系統提供的網絡服務。例如,操作系統通過套接字(Socket)接口為應用程序提供網絡通信能力,使得HTTP等協議能高效運行。
5. 期末考試重點提示
- 掌握HTTP請求-響應模型及報文結構。
- 理解DNS在應用層中的作用。
- 熟悉常見應用層協議(如FTP用于文件傳輸,SMTP用于電子郵件)的對比。
- 結合實例分析應用層如何通過系統服務實現網絡通信。
通過以上圖解和解析,應用層的核心概念一目了然。復習時多練習協議交互流程圖和報文分析,就能在考試中游刃有余。記住,應用層是網絡應用的橋梁,扎實掌握它,計算機網絡學習就成功了一半!